4 – Impédance ou Résistance Circulatoire
L’impédance ou résistance circulatoire
1 – L’onde artérielle et ses conséquences
Les variations de vitesse d’écoulement du sang dans les artères au cours du cycle cardiaque, telles qu’elles peuvent être enregistrés par l’effet Doppler, suivent une modulation qui résulte du caractère pulsé de l’écoulement généré, à chaque systole, par la contraction ventriculaire, et du rôle particulier joué par la souplesse de la paroi artérielle, fonctionnant comme un amortisseur.
La souplesse de la paroi artérielle est en effet déterminante dans la transformation du flux aortique pulsé en un écoulement capillaire continu. Cette transformation est assurée par le dispositif constitué par les valves cardiaques, la résistance circulatoire périphérique, et l’élasticité de la paroi artérielle. A chaque éjection systolique, en effet, la paroi artérielle (en commençant par l’aorte initiale) se laisse distendre et stocke provisoirement une large part du volume d’éjection systolique, car le niveau de la résistance circulatoire périphérique ne permet pas d’écouler un tel volume dans le seul temps que dure la systole. Une large part (plus des deux tiers) du volume sanguin éjecté du ventricule s’écoule donc perpendiculairement au grand axe du vaisseau (composante radiale, ou transversale, de l’écoulement). Le volume sanguin ainsi stocké est restitué, par retour de la paroi artérielle à sa position de repos, dès la fin de l’éjection systolique, donnant lieu à un écoulement axial. Ce phénomène se propage de proche en proche le long de la paroi artérielle jusqu’en périphérie, constituant l’onde artérielledont la manifestation la plus connue est lepouls. Son mécanisme et son intérêt ont été initialement décrits par Stephen Hales, en 1733, par analogie au réservoir d’air (« Windkessel », en allemand) qui équipait les pompes à bras avec lesquelles on luttait, autrefois, contre les incendies. Dans le modèle proposé par Hales (et affiné depuis), le secteur veineux constitue un réservoir sanguin, le ventricule et son dispositif valvulaire forment une pompe intermittente, les artères représentent un circuit de distribution (tuyaux), et les artérioles constituent une résistance circulatoire variable (l’extrémité réglable de la lance), tandis que l’élasticité de la paroi artérielle, capable de stocker temporairement volume et pression, fonctionne à l’instar de la « cloche à air » permettant de régulariser le débit.
L’onde artérielle se réfléchit sur diverses « singularités » de l’arbre artériel, c’est-à-dire sur toutes les zones où la géométrie ou les caractéristiques mécaniques de l’artère font l’objet d’un changement brusque. Les embranchements et bifurcations, mais aussi l’ensemble des artérioles (de par l’accroissement de résistance à l’écoulement qu’elles occasionnent) constituent donc autant de sites de réflexion.
L’onde réfléchie revient donc vers le cœur, et vient interférer avec l’onde incidente (par un jeu d’ondes « stationnaires »), pour marquer clairement la modulation des vitesses circulatoires (« tracé Doppler »). Elle contribue aussi à la fermeture des valves sigmoïdes aortiques, et à la perfusion des artères coronaires (puisque celle-ci n’est pas possible dans de bonnes conditions en systole, le myocarde ventriculaire étant contracté).
2 – La modulation du tracé de vitesse circulatoire
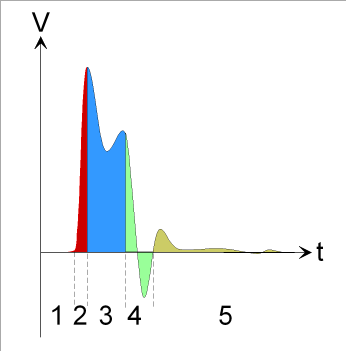
Ainsi, le « tracé Doppler » montre, sur une artère normale, une succession d’événements en relation avec le cheminement de l’onde artérielle(fig. 25) :
Figure 25: Modulation du tracé Doppler normal d’une artère périphérique : après un délai (1) fonction de la distance séparant du cœur le site de mesure Doppler, l’arrivée de l’onde artérielle provoque une accélération dite « systolique » (2), suivie d’une décélération marquée par une incisure (3) traduisant le retour de l’onde réfléchie, puis d’une onde négative (4) pouvant, sur les artères destinées à un territoire de haute résistance circulatoire, constituer une véritable inversion circulatoire. Le niveau de vitesse télédiastolique dépend de la résistance circulatoire d’aval.
- Une première phase, de latence, sépare l’éjection systolique (repérée, par exemple, par le complexe QRS sur l’électrocardiogramme) de l’arrivée de l’onde artérielle au site d’enregistrement Doppler. Sa durée est fonction de la vitesse de propagation de l’onde artérielle et de la distance parcourue (donc de la distance à l’orifice aortique).
- Une phase dite d’accélération systolique, constituant le front de montée (pente ascendante) du pic systolique, et correspondant à l’accélération de l’écoulement sanguin provoquée par l’arrivée de l’onde artérielle.
- Une phase descendante du pic systolique, ou décélération, marquée par une incisure dicrote qui correspond à l’arrivée de l’onde réfléchie. C’est à partir de cet instant que la courbe de vitesses d’écoulement du sang (« tracé Doppler ») se différencie de la courbe de pression. Alors que la réflexion de l’onde de pression donne lieu à un rehaussement transitoire de la pression sanguine locale après le pic systolique, l’onde de vitesse réfléchie est orientée vers le cœur, de sorte qu’elle vient se soustraire à l’onde incidente. C’est pourquoi le tracé de vitesse d’écoulement du sang se présente comme la dérivée du tracé de pression.
- Une phase d’inversion circulatoire post-systolique transitoire. Cette phase apparaît en fait comme une profonde encoche sur le versant descendant du pic systolique sur les artères irriguant un territoire qui offre une résistance circulatoire faible, et l’écoulement reste orthograde pendant tout le cycle cardiaque. Par contre, sur les artères irriguant un territoire offrant une forte résistance à l’écoulement, survient une véritable inversion du sens circulatoire en début de diastole.
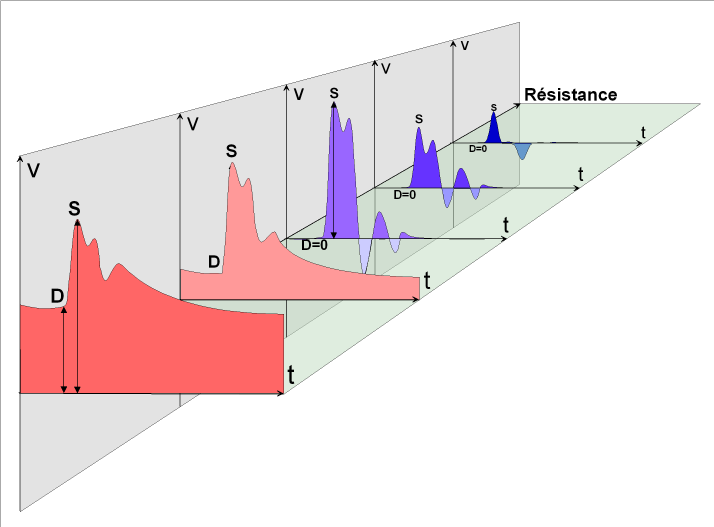
- Le reste du tracé, qui correspond à la diastole (artérielle) dépend aussi du niveau de résistance d’aval à l’écoulement. Sur les artères destinées à un territoire de basse résistance circulatoire, cette phase comporte un flux orthograde se ralentissant progressivement (pente descendante douce) mais restant présent en fin de diastole. Sur les artères destinées à un territoire de haute résistance circulatoire, l’écoulement s’interrompt rapidement en début de diastole, et reste nul par la suite jusqu’à la systole suivante(fig. 26).
Figure 26: La modulation du tracé de vitesse circulatoire artériel, au Doppler, dépend de la résistance circulatoire dans le territoire irrigué par l’artère examinée : le flux diastolique est d’autant plus grand, en comparaison du flux systolique, que la résistance circulatoire d’aval est faible. Inversement, si la résistance circulatoire d’aval est élevée, le flux s’interrompt dès le début de la diastole.
3 – Impédance et résistance circulatoire
La modulation du tracé de vitesses circulatoires sanguine enregistré, sur les artères, par effet Doppler reflète donc les conditions hémodynamiques générales et locales. En particulier, l’importance relative de la vitesse diastolique en comparaison de la vitesse maximale systolique est liée au niveau de résistance circulatoire dans le territoire d’aval. En théorie, cette résistance à l’écoulement dépend aussi de l’accélération, de sorte qu’il conviendrait de parler d’impédance et non de résistance. Néanmoins, dans les conditions courantes, cette approximation est cliniquement acceptable.
En pratique, donc, l’observation de la modulation du tracé de vitesses circulatoires d’une artère permet d’évaluer la résistance circulatoire d’aval(9). Sur ces observations sont fondés lesindices, grandeurs sans dimensions proposées, dès les premières années d’application de l’effet Doppler à l’étude de la circulation sanguine, par Léandre Pourcelot d’une part, Raymond Gosling d’autre part(fig. 27).
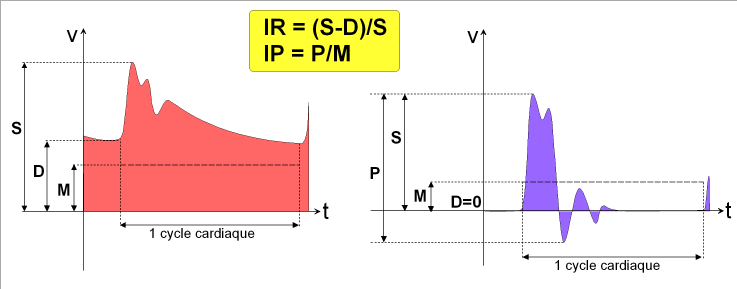
– L’indice de Résistance, proposé par L Pourcelot, s’écrit IR = (S-D)/s, avec S = vitesse maximale systolique, et D = vitesse maximale télé-diastolique.
– L’indice de Pulsatilité, proposé par R Gosling, s’écrit IP = P/M, avec P = amplitude maximale du tracé (de la plus haute valeur positive, c’est-à-dire du sommet du pic systolique, à la plus basse valeur, c’est-à-dire au nadir de la phase éventuelle d’inversion circulatoire (ou « reflux ») en début de diastole ou de la vitesse télé-diastolique, et M = vitesse circulatoire moyenne, la moyenne étant calculée sur la totalité du cycle cardiaque.
Figure 27: L’indice de résistance IR(à gauche) convient bien à l’évaluation des conditions hémodynamiques sur les artères à basse résistance circulatoire d’aval, comme les artères cérébrales. L’indice de pulsatilité IP (à droite) est bien adapté à l’évaluation des artères à haute résistance circulatoire d’aval, comme les artères des membres.
Ces deux indices évoluent dans le même sens : ils augmentent lorsque la résistance circulatoire d’aval augmente, diminue si elle décroît.
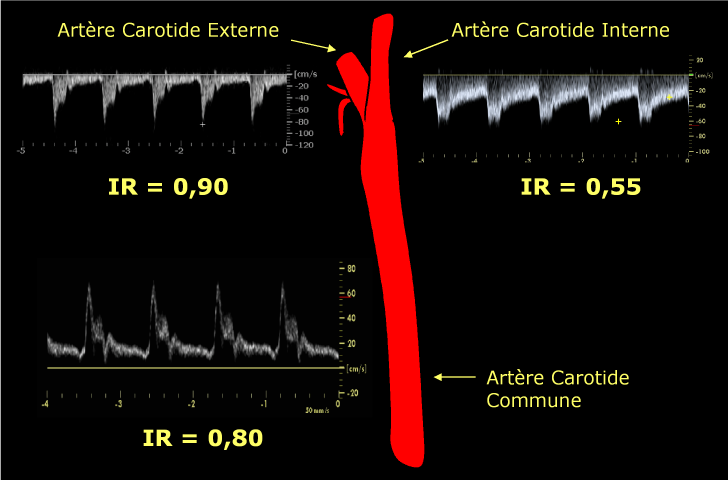
C’est ainsi que l’on peut reconnaître des artères dont le tracé Doppler, chez le sujet normal, est caractéristique d’une faible résistance circulatoire d’aval, comme la carotide interne, l’artère vertébrale, l’artère rénale, tandis que d’autres, comme la carotide externe ou les artères des membres au repos, présentent un tracé évocateur d’un territoire à forte résistance circulatoire(fig. 28).
Figure 28: Chez un sujet sain, l’artère carotide interne présente un tracé Doppler caractéristé par un indice de résistance bas, tandis que l’indice de résistance est élevé sur la carotide externe, et intermédiaire sur la carotide commune.
De plus, ces indices peuvent rendre compte des variations de résistance circulatoire :
– Transitoires, du fait de la vasomotricité : par exemple, les vitesses circulatoires augmentent fortement, particulièrement pour ce qui est de la vitesse diastolique, lors d’un effort musculaire comme, par exemple, des flexions – extensions sur la pointe des pieds pour l’artère fémorale. De même, l’hyperventilation volontaire, par le biais de l’hypocapnie entraînant une vasoconstriction cérébrale, modifie le tracé de la carotide interne dont la vitesse diastolique diminue significativement, alors qu’elle augmente, comparativement à la vitesse systolique, lors d’une apnée.
– Permanentes, en cas d’obstacle circulatoire d’aval comme une sténose significative ou une occlusion, qui, introduisant une résistance circulatoire additionnelle, augmentent l’indice de résistance et l’indice de pulsatilité. Inversement, en aval d’une sténose ou d’une occlusion, la vasorelaxation réactionnelle à l’ischémie réduit la résistance circulatoire et diminue donc la valeur de ces indices.
L’indice de résistance comme l’indice de pulsatilité doivent être déterminés sur la courbe de vitesse maximale, et non moyenne.
En pratique, l’indice de résistance est très « robuste » : de détermination rapide et facile, il peut être mesuré aisément en toutes circonstances. Par contre, il ne rend pas compte des différences éventuelles entre artères dès lors que la vitesse télé-diastolique est nulle. L’indice de résistance est alors égal à 1, que la vitesse circulatoire soit nulle dès le début de la diastole ou qu’elle le devienne simplement en fin de diastole(fig. 68). Une variante de calcul consiste à prendre, sur les artères qui présentent une phase de reflux, la plus basse valeur négative éventuelle pour déterminer D, conduisant alors à obtenir un indice supérieur à 1. Ce mode de calcul, en de telles circonstances, permet d’affiner un peu la sensibilité de l’indice de résistance pour les artères à haute résistance circulatoire d’aval.
L’indice de pulsatilité est plus sensible dans cette gamme de valeur, puisqu’il prend en compte la moyenne temporelle de vitesse circulatoire. Cependant, sa détermination nécessite un calcul automatique de la ligne de vitesse maximale et son moyennage sur un nombre entier de cycles cardiaques (moyenne temporelle de vitesse maximale). Tous les appareils ne sont pas capables d’effectuer ce calcul dans de bonnes conditions. Si ce n’est pas le cas, il est préférable d’utiliser l’indice de résistance, plutôt que de perdre de longs moments à suivre manuellement l’enveloppe supérieure du tracé pour obtenir, laborieusement, un résultat subjectif et approximatif.
D’autres indices et valeurs chiffrées ont été proposés pour décrire la modulation du signal Doppler. Les plus pertinents sont relatifs à la pente ascendante du pic systolique : mesure de l’accélération (en cm.s-2), ou, plus simplement, du temps d’accélération (en ms), dit aussi « temps d’ascension systolique ». La détermination de ces valeurs est plus délicate, et il importe de mesurer l’accélération sur la phase initiale, la plus raide, de la pente ascendante du pic systolique. En aval d’un obstacle circulatoire, qui intervient sur la modulation du signal Doppler comme un filtre, cette pente est en effet amoindrie, et le temps d’ascension est prolongé, tandis que la modulation du tracé est estompée. A l’extrême, le signal peut perdre quasiment toute modulation (par exemple en aval d’un embole) et devenir presque continu. En pratique, la mesure du temps d’ascension systolique est facile et précise lorsque le pic systolique est net, acuminé, c’est-à-dire normal. Elle est beaucoup plus imprécise lorsque son sommet est arrondi (« amorti »), donc en aval d’un obstacle. La mesure de l’accélération systolique est donc préférable, mais n’est possible que si l’angle d’incidence peut être mesuré avec précision (et, naturellement, s’il est inférieur à 60°). Enfin, l’accélération systolique ne peut être correctement interprétée qu’en référence aux conditions hémodynamiques générales, en particulier aux caractéristiques de l’éjection systolique. A cet égard, l’accélération systolique est plus forte chez le sujet jeune, moindre chez le sujet âgé, et significativement ralentie, sur l’ensemble du réseau artériel, en cas d’insuffisance cardiaque gauche et/ou de rétrécissement aortique.