3A – Etat de la paroi artérielle
Etat de la paroi artérielle
Si, usuellement, l’examen ultrasonographique n’est exploité que pour l’étude morphologique de la paroi artérielle, il est capable d’apporter en outre de précieux renseignements sur son état biomécanique et fonctionnel.
1 Etude morphologique
1.1 La paroi artérielle normale
L’examen histologique de la paroi artérielle montre trois couches :
– Au contact du sang circulant dans la lumière, l’intima, formé par l’endothélium (couche monocellulaire) reposant sur une assise conjonctive.
– Lamédia, constituée de cellules musculaires lisses disposées de façon hélicoïdale au sein d’une matrice d’élastine et de collagène, et séparée de l’intima d’une part, de l’adventice d’autre part, par une couche conjonctive, la « limitante élastique ».
– L’adventice, couche conjonctive.
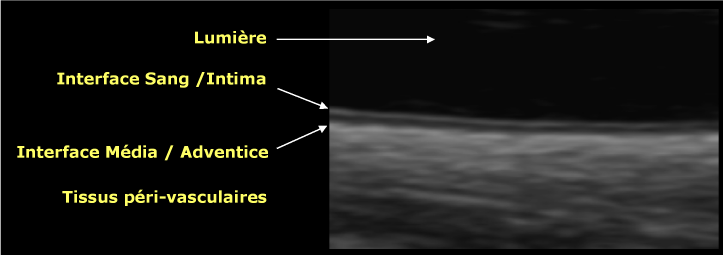
L’image échographique ne montre pas ces couches histologiques, mais les interfaces qu’elles constituent(fig. 7) :
– L’interface sang / intima, donnant une image de fin liseré de tonalité grise. L’épaisseur de ce liseré dépend principalement de l’échogénicité de l’interface et de la résolution spatiale axiale de l’échographe. Elle est donc sans rapport ni proportion avec l’épaisseur de l’intima, qui n’est que de quelques µm tout au plus. L’écho de l’interface sang / intima masque donc celui de l’interface intima / média (qui est du reste peu réfléchissante).
– L’interface média / adventice, donnant un liseré brillant et plus épais.
– Entre ces deux liserés, se trouve donc délimitée une bande hypo- ou anéchogène dont l’épaisseur est proportionnelle à la média (déduction faite de l’épaisseur de l’écho de l’interface sang / intima,cf. supra). La média est proportionnellement plus épaisse sur les artères distales, dites « musculaires » que sur les artères proximales (comme les carotides, l’artère brachiale…) dites « élastiques ». Cependant, son épaisseur en valeur absolue diminue lorsque l’on s’éloigne du cœur, tandis que l’épaisseur du liseré produit par l’interface sang / intima change peu (puisqu’elle dépend fortement de la résolution axiale), de sorte que l’épaisseur apparente de cette bande intermédiaire hypo-échogène est sans rapport direct avec l’épaisseur réelle de la média.
Figure 7: Image échographique de la paroi d’une artère carotide commune normale (versant profond), montrant l’interface sang / intima et l’interface média / adventice.
En temps réel, l’échographie peut montrer le discret glissement systolique longitudinal du liseré externe par rapport aux tissus environnants. Cependant, le mouvement de la paroi artérielle est dominé par la pulsatilité radiale (ou transversale) de l’artère, démontrant le passage de l’onde de pouls (cf.ce chapitre).
On peut noter que, sur une artère normale, la lumière, bien perméable, apparaît anéchogène (hormis avec les sondes de très haute fréquence, qui permettent de visualiser le flux, notamment en mode harmonique). En revanche, le liseré externe de l’artère (interface média / adventice) est très échogène. Il est donc possible, en pratique, de se fonder sur ces niveaux d’échogénicité pour régler le gain et la dynamique de l’appareil d’échographie lors de l’examen artériel. Le réglage est correct lorsque la lumière apparaît vide d’échos (noire sur l’image, c’est-à-dire à un niveau proche de 0 sur l’échelle de gris, qui en comporte généralement 256), tandis que le liseré externe de l’artère apparaît brillant, presque blanc, sans saturation (proche du 256èmeet dernier niveau de l’échelle de gris, sans cependant l’atteindre). Ainsi, le liseré interne de l’artère (interface sang / intima) doit apparaître d’un gris intermédiaire, à mi-chemin de ces deux extrêmes.
1.2 Descriptiondes plaques
Les plaques d’athérome constituent les lésions les plus fréquentes de la paroi artérielle, et l’échographie permet leur analyse séméiologique simple, reposant sur la description de leur site, de leurs mensurations, de leur échostructure, de leur surface, et de leur échogénicité(fig. 8). Ces caractéristiques ont été particulièrement étudiées sur les artères carotides, parce qu’elles sont cliniquement pertinentes, mais aussi parce que les conditions d’examen à ce niveau sont généralement favorables (il est, par exemple, beaucoup plus difficile voire impossible de donner une description fine de plaques éventuelles sur les artères rénales, plus profondes et donc hors de portée des sondes de haute fréquence offrant la résolution nécessaire).
– Site et dispositionde la plaque : l’angiosonologiste doit décrire avec précision, à partir de coupes longitudinales, l’emplacement de la plaque, et, à partir de coupes transversales, sa disposition (localisée sur un versant artériel ou circonférentielle, centrée ou excentrée). Les plaques étant le plus souvent situées à proximité d’une bifurcation, il est d’usage de déterminer leur distance et leur étendue par rapport à cette bifurcation. Il faut ensuite en donner les principales mensurations : étendue selon le grand axe du vaisseau, et épaisseur maximale.
– Surface : la plaque peut apparaître de surface lisse, régulière, ou, au contraire, complexe, irrégulière, anfractueuse. Dans ce cas, il est utile de mesurer la profondeur d’un éventuel cratère à la surface de la plaque.
– Echogénicité : la plaque peut comporter des composants hypo- ou anéchogènes(fig. 8), iso-échogènes(fig. 9), ou hyper-échogènes(fig. 10). En pratique, le niveau d’échogénicité peut être évalué par comparaison à celui du liseré interne normal de l’artère, considéré comme « iso-échogène ». Les composants plus échogènes que ce liseré normal sont ainsi dits « hyper-échogènes », et les composants moins échogènes sont dits « hypo-échogènes ». Une précision supplémentaire s’applique aux composants hyper-échogènes, qui peuvent s’accompagner ou non d’une ombre acoustique (toute l’énergie acoustique étant réfléchie par la plaque, aucune structure ne peut être visualisée au-delà)(fig. 11).
– Echostructure : la plaque peut apparaître de structure interne uniforme ou hétérogène(fig. 12).
Figure 8: Plaque très hypoéchogène, de surface lisse, sur le versant antéro-latéral de la bifurcation carotidienne. Le Doppler en mode énergie permet de délimiter cette plaque, à peine visible sur l’échographie en mode B.
Figure 9: Petite plaque lisse iso-échogène et homogène sur le versant antério-latéral de la bifurcation carotidienne, avec une délimitation nette (cape fibreuse) par rapport à lumière artérielle.
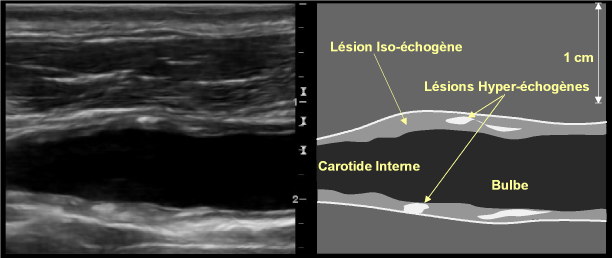
Figure 10: Plaque circonférentielle, peu épaisse, de surface lisse, au niveau du bulbe carotidien, montrant des composants hyper-échogènes sans ombre acoustique, au sein d’un épaississement iso-échogène de la paroi.
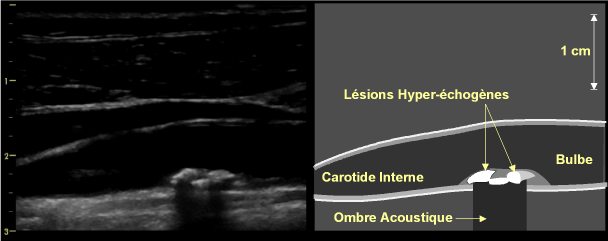
Figure 11: Plaque peu épaisse, de surface relativement régulière, sur le versant postéro-médial de la bifurcation carotidienne, avec une composition majoritairement hyper-échogène et calcifiée, se traduisant par une large ombre acoustique.
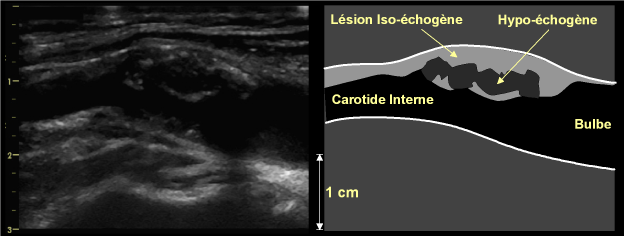
Figure 12: Plaque volumineuse, circonférentielle prédominant sur le versant antéro-latéral de la bifurcation carotidienne, avec une composition très hétérogène, mêlant des zones hypo- et des zones iso-échogènes, avec une surface irrégulière et mal délimitée.
1.3 Interprétationdes images échographiques des plaques
Il n’existe pas de séméiologie échographique univoque des plaques d’athérome, mais quelques repères d’analyse qui ne peuvent être interprétés qu’en prenant en compte le tableau clinique.
– Les composants hypo-échogènes d’une plaque peuvent correspondre à des dépôts lipidiques confluents (plaques « jeunes »), ou à une hémorragie au sein de la plaque, ou à une nécrose. Ces deux dernières situations sont plutôt (mais pas uniquement) le fait de plaques plus anciennes mais non « cicatricielles » mais « instables », remaniées.
– Les composants iso-échogènes peuvent résulter d’un remaniement fibreux (encerclement) des dépôts lipidiques au sein de la paroi artérielle.
– Les composants hyper-échogènes résultent généralement d’une fibrose extensive (constituant une forme de stabilisation).
– La survenue d’une calcification se signale par une ombre acoustique.
Les caractéristiques de surface de la plaque ne peuvent pas, non plus, faire l’objet d’une interprétation univoque. Une surface irrégulière, anfractueuse, y compris lorsqu’elle montre un profond cratère, ne permet pas d’affirmer l’existence d’une ulcération, car celle-ci se définit comme l’effraction de l’endothélium, dont l’épaisseur est de loin inférieure à la résolution spatiale des meilleurs appareils. Le diagnostic d’ulcération ne peut donc pas être affirmé, mais sa probabilité est, évidemment, plus grande lorsque la plaque apparaît anfractueuse,a fortiorichez un patient symptomatique.
En pratique, c’est l’échogénicité de la plaque qui constitue le critère majeur en rapport avec le risque clinique qu’elle représente. Ce risque est en effet d’autant plus grand que la plaque est majoritairement hypo-échogène,a fortiorisi elle détermine une sténose significative.
Hypo-échogénicité et degré de sténose sont donc les deux déterminants majeurs du risque clinique de la plaque, généralement parce qu’elle peut alors être à l’origine de la migration d’emboles. De fait, le risque de rupture du revêtement endothélial est d’autant plus grand que la plaque est déformable (ce qui est le cas d’une plaque hypo-échogène) et qu’elle est soumise à des contraintes mécaniques importantes (ce qui est le cas en présence d’une sténose, dès lors que, en vertu de la Loi de Bernoulli, la pression sanguine est abaissée dans le jet de la sténose, et accrue en aval, lorsque le diamètre de la lumière augmente à nouveau, surtout s’il existe une dilatation post-sténotique). Inversement, une plaque non-sténosante majoritairement hyper-échogène, voire calcifiée, présente un moindre risque car moins fragile et moins sollicitée.
Ces notions n’ont cependant qu’une valeur relative, ce que démontre quotidiennement la confrontation aux données cliniques.
1.4 Lamédiacalcose
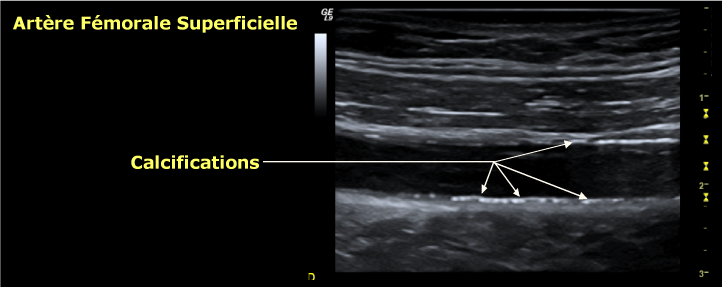
Les calcifications de la média de la paroi artérielle (médiacalcose de Monckeberg) sont à l’origine des images parmi les plus fréquentes, voire banales, en échographie vasculaire. Particulièrement fréquentes chez le diabétique et l’insuffisant rénal chronique, ces images sont celles de calcifications dans l’épaisseur – même de la paroi(fig. 13). A ce titre, elles doivent être bien distinguées d’éventuelles calcifications au sein de plaques d’athérome, dont la signification est bien différente.
Figure 13: Médicalcose de l’artère fémorale superficielle, se traduisant par des images discontinues (en pointillés) dans l’épaisseur de la paroi (au sein de la média), sans altération de la lumière.
La médiacalcose prédomine généralement sur la paroi des artères des membres inférieurs, en particulier à partir de la fémorale superficielle, en augmentant vers l’extrémité du membre. On les retrouve parfois au membre supérieur, notamment chez l’insuffisant rénal chronique.
Apparaissant initialement comme des images en pointillés hyper-échogènes au sein de la paroi, avec autant d’ombres acoustiques, ces lésions peuvent devenir confluentes et aboutir à la calcification « en masse » de la paroi artérielle sur tout un segment. L’examen de la lumière devient alors difficile, voire impossible, et cela peut être à l’origine de faux diagnostics d’occlusion.
En outre, la médiacalcose est susceptible de fausser la mesure de pression artérielle systolique à la cheville, ce qui constitue un écueil fréquent de cette mesure. Dans les cas sévères, les artères de jambe sont incompressibles, de sorte qu’il n’est pas possible, lors du gonflement du garrot pneumatique, d’obtenir la disparition du signal Doppler en aval. La mesure de pression n’est alors pas réalisable, et il convient d’effectuer la mesure à l’orteil. Dans les formes intermédiaires, le risque diagnostique est plus gênant, car la mesure peut donner des valeurs faussement élevées. En pratique donc, la constatation d’une médiacalcose significative doit faire mettre en question la fiabilité de la mesure de pression artérielle systolique à la cheville, et doit lui faire préférer la mesure à l’orteil.
1.5 Ladissectionde la paroi artérielle
Au stade aigu, une dissection de la paroi artérielle peut apparaître sur l’image échographique :
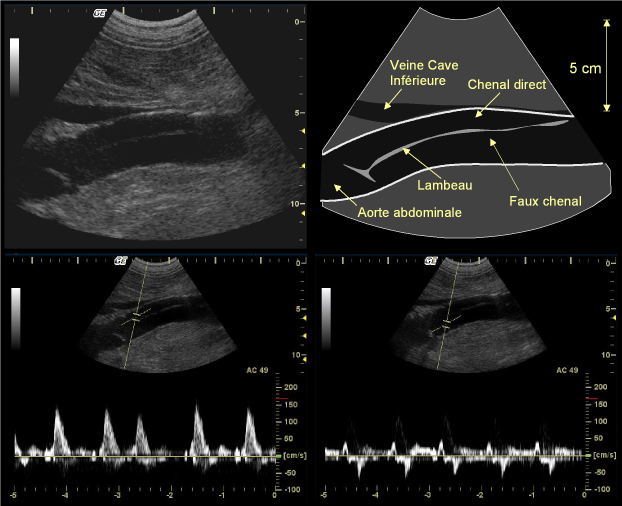
– Soit sous la forme d’un lambeau échogène au sein de la lumière artérielle, délimitant deux chenaux(fig. 14). L’examen Doppler montre alors que le signal recueilli dans chacun de ces chenaux est différent, avec un décalage de phase très net entre les deux chenaux (le pic systolique est retardé dans le faux chenal). De plus, le signal Doppler est souvent remanié, avec un pic systolique bifide, résultant du déplacement systolique du lambeau de dissection, du fait que celui-ci subit de part et d’autre des variations de pression asynchrones. Ce tableau correspond à l’image d’une dissection sous-intimale.
Figure 14: Dissection aortique étendue à l’aorte abdominale. L’échographie en coupe longitudinale montre le lambeau mobile divisant la lumière et délimitant deux chenaux parallèles, dont l’un est le siège d’un flux anormal, avec une modulation profondément altérée.
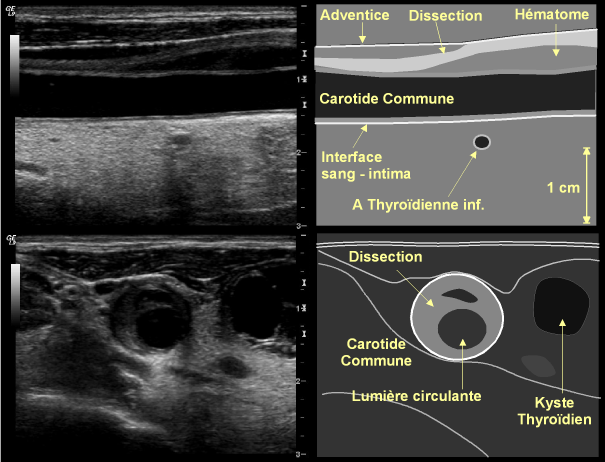
– Soit sous la forme d’un élargissement localisé de l’artère, qui montre une voussure externe par un épaississement iso-échogène au sein de la paroi, tandis que l’interface sang / intima reste bien visible et régulière, bien que bombant souvent dans la lumière (qui se trouve ainsi rétrécie). Ce tableau est en faveur d’une dissection sous-adventicielle(fig. 15).
Figure 15: Dissection sous-adventicielle spontanée de la carotide commune (chez une jeune femme porteuse, par ailleurs, de kystes thyroïdiens). Noter, sur l’image en coupe longitudinale (en haut) et transversale (en bas), l’hématome pariétal créant une voussure.
Les images échographiques ne sont cependant pas souvent aussi évidentes. L’un des chenaux peut être thrombosé. Le lambeau mobile peut rester invisible (en particulier lorsque l’artère, relativement profonde, ne peut être examinée avec une sonde de fréquence suffisamment haute). Le mode harmonique peut améliorer considérablement la visualisation du lambeau.
A un stade plus tardif, l’interprétation des images est beaucoup plus difficile, et repose avant tout sur les données cliniques. Lorsqu’il persiste une occlusion totale de l’artère, celle-ci n’est pas toujours aisément distinguable d’une occlusion « banale » athéro-thrombotique, hormis lorsque la voussure externe de l’artère plaide en faveur d’une dissection sous-adventicielle,a fortiorisi les axes artériels sont par ailleurs indemnes de lésions athéromateuses.
Dans les dissections sous-intimales, lorsque l’artère est restée perméable, le lambeau s’épaissit généralement, et ses mouvements systoliques diminuent ou disparaissent, tandis que les anomalies du signal Doppler persistent.
Enfin, l’évolution vers une dilatation anévrismale est classique et doit faire l’objet d’une surveillance régulière avec des mensurations précises.
1.6 Lesartéritesinflammatoires et radiques
Au stade aigu, les artérites inflammatoires se signalent sur les images échographiques par l’épaississement marqué et étendu, iso-échogène, de la paroi artérielle, donnant lieu, bien souvent, à des sténoses très longues et régulières.
Néanmoins, l’interprétation se fonde tout autant sur le contexte (l’âge, l’ethnie, le syndrome inflammatoire éventuel) et sur la répartition des lésions pour évoquer le diagnostic.
Les lésions anciennes perdent leur spécificité, notamment en cas d’obstruction totale, avec d’importants remaniements fibreux échogènes. Les données cliniques n’en sont que plus importantes.
Les lésions consécutives à une radiothérapie sont de plus en plus rares, car les oncologues déterminent des champs d’irradiation de plus en plus précis. Les localisations principales sont la carotide (après irradiation pour tumeur de la sphère ORL, en particulier du larynx) ainsi que l’artère subclavière, l’artère axillaire, et l’artère brachiale (après irradiation pour cancer du sein). L’artérite post-radiothérapie (dite « radique ») se manifeste par un épaississement iso- ou discrètement hyper-échogène étendu de la paroi artérielle(fig. 16). Le contexte et les antécédents aident au diagnostic, mais la coexistence de lésions athéromateuses « banales » peut rendre l’analyse difficile, notamment chez un patient opéré d’une tumeur ORL, avec, bien souvent, des antécédents de tabagisme important.
Figure 16: Artérite « radique » : épaississement pariétal étendu, iso-échogène, de la carotide commune chez un patient ayant des antécédents de radiothérapie pour cancer de l’œsophage.
1.7 Lesdysplasiesde la paroi artérielle
Typiquement, l’image échographique d’une paroi artérielle dysplasique est marquée par son caractère irrégulier, avec une mauvaise différenciation des deux interfaces, un calibre souvent réduit (lumière effilée), et, dans les cas les plus démonstratifs, un image en accordéon ou en soufflet.
Cependant, bien souvent, l’examen reste décevant, principalement pour des raisons techniques, car la situation des lésions (carotide interne haute, artère rénale distale…) ne permet pas de les examiner dans les meilleurs conditions.
En outre, l’angiosonologiste est le plus souvent confronté à ces lésions lorsqu’elles ont eu une manifestation clinique, notamment en ce qui concerne les artères carotides. Dès lors, l’image d’occlusion artérielle peut paraître banale, et les autres techniques d’imagerie (en particulier l’IRM) sont plus performantes. Par contre, le diagnostic peut être plus facilement évoqué sur l’artère rénale, lorsque l’examen démontre une sténose distale chez une femme jeune.
1.8 Les anomalies decalibreet de longueur
L’anévrismeest une anomalie localisée du calibre de l’artère, donnant naissance à une dilatation coaxiale (anévrisme fusiforme) ou extra-axiale (anévrisme sacciforme). Au niveau de l’anévrisme, la paroi peut rester apparemment saine, ou être tapissée d’une lame plus ou moins épaisse de thrombose(fig. 17). Cette dernière apparaît comme un matériel iso-échogène, parfois hétérogène lorsque qu’elle est remaniée avec des zones d’hémorragie ou de nécrose. La thrombose est parfois obstructive, lorsqu’elle réduit significativement la lumière perméable. Au sein de l’anévrisme, le signal Doppler peut présenter des altérations évocatrices (cf. infra). La thrombose peut être totale, ce qui représente une complication classique de certains anévrismes (notamment au niveau de l’artère poplitée), mais peut aussi être à l’origine de migrations emboliques itératives dans le lit d’aval.
Figure 17: Coupe échographique transversale d’un anévrisme fusiforme de l’aorte abdominale, avec une thrombose partielle semi-circonférentielle.
Les autres complications de l’anévrisme, comme la fissuration, peuvent plus rarement être diagnostiquées par l’examen écho-Doppler, et justifient donc le recours à l’imagerie radiologique en coupes.
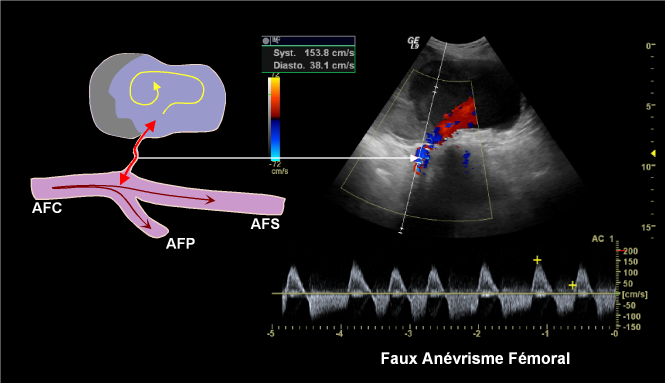
Notons que lefaux-anévrismeest une entité bien différente. Il résulte d’une brèche dans la paroi artérielle avec constitution d’un hématome circonscrit au sein duquel circule un flux sanguin tourbillonnant (souvent visible en raison de l’agrégation érythrocytaire consécutive à la stase sanguine). Le chenal qui conduit de la lumière artérielle à la lésion est le siège d’un flux alternant caractéristique, le faux-anévrisme se remplissant en systole et se vidant ensuite, pendant toute la durée de la diastole(fig. 18).
Figure 18: Faux anévrisme fémoral après cathétérisme artériel pour coronarographie. Noter le flux alternant caractéristique : positif en systole (remplissage du faux-anévrisme), puis négatif pendant toute la durée de la diastole (vidange).
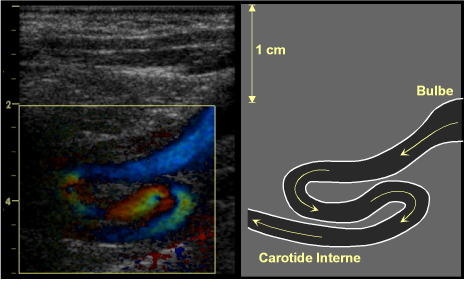
Lesbouclesartérielles sont une constatation banale, en particulier chez la personne âgée. Particulièrement fréquentes sur la carotide interne(fig. 19), elles peuvent aussi concerner l’artère vertébrale, le tronc brachio-céphalique, les artères fémorales ou brachiales. Elles ne posent pas de difficulté diagnostique à l’écho-Doppler, mais imposent un examen attentif afin d’identifier le trajet de l’artère, imposant la réalisation de coupes sous de multiples incidences. Les méga-dolicho-artères s’observent dans le même contexte. L’allongement de l’artère (responsable de sinuosités et boucles) s’accompagne alors d’une augmentation globale de calibre.
Figure 19: Boucle de la carotide commune, sans obstacle circulatoire.
Bien qu’elles représentent une notion classique, lesplicaturesartérielles sont plus rares, et plus rarement encore responsables de troubles cliniques.
1.9 Leslésions tumoralesde la paroi artérielle
Les tumeurs de la paroi vasculaire sont exceptionnelles, et leur rareté ne permet pas d’en donner une description séméiologique précise.
Par contre, les tumeurs glomiques, (lésions rares, survenant principalement dans la bifurcation carotidienne, assez souvent bilatérales et familiales), présentent un aspect ultrasonographique évocateur : l’échographie montre une masse hypo-échogène hétérogène écartant les branches de la bifurcation, tandis que le Doppler couleur montre une hypervascularisation artérielle et veineuse globale, et que le Doppler pulsé enregistre des flux artériels intenses, de hautes vitesses circulatoires et de bas indice de résistance, avec des flux veineux rapides à renforcement systolique.
1.10 La paroi artérielle aprèsendartériectomie
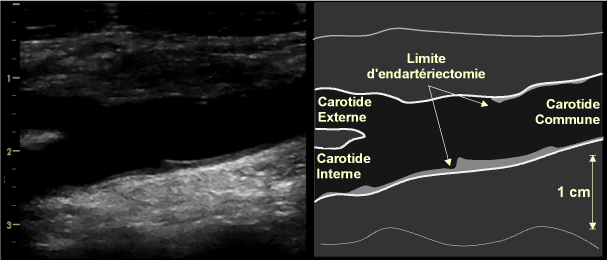
L’observation de la paroi artérielle après endartériectomie concerne essentiellement les artères carotides. Le chirurgien « clivant » littéralement la paroi artérielle au niveau de la média, l’aspect de la paroi est ensuite modifié, l’interface sang / intima n’étant plus visible. Il en résulte un aspect en « marche d’escalier » à la limite d’endartériectomie, d’autant plus si la paroi de part et d’autre de la zone opérée présente un épaississement pariétal ou une plaque. On constate en outre la disparition du galbe normal de l’artère, donnant à la zone opérée un aspect boursouflé(fig. 20). Enfin, les sutures sont souvent bien visibles avec les sondes de haute résolution.
Dans les jours qui suivent l’opération, les complications que peut montrer l’échographie sont la thrombose partielle ou totale (un amas échogène obstruant en tout ou partie la lumière), la présence d’un lambeau intimal décollé, flottant dans la lumière, ou encore un hématome : collection péri-artérielle hypo- ou anéchogène, mais devenant rapidement hétérogène lorsque la thrombose s’installe. Plus rarement, un faux-anévrisme se signale par la présence d’un flux tourbillonnant au sein d’un hématome, avec une brèche dans la paroi et, le long du chenal amenant à l’hématome, un flux typique en va-et-vient (cf. supra).
Figure 20: Image échographique, en coupe longitudinale, de la bifurcation carotidienne 2 mois après une endartériectomie : noter l’aspect en « marche d’escalier » à l limite d’endartériectomie, et la perte du galbe régulier du bulbe carotidien.
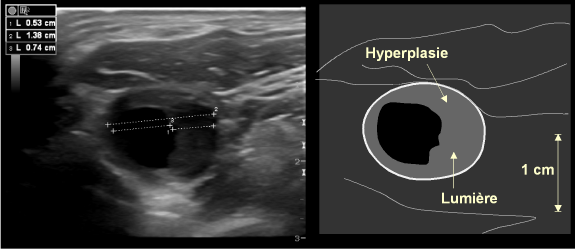
Dans les premiers mois qui suivent l’endartériectomie, l’hyperplasie myo-intimale est la première cause de récidive de sténose. Elle se présente comme un épaississement pariétal hypo- ou iso-échogène prédominant au niveau des limites d’endartériectomie(fig. 21).
Figure 21:Image, en coupe transversale, du bulbe carotidien 6 mois après une endartériectomie, montrant une hyperplasie myointimale marquée, iso-échogène, sans sténose hémodynamiquement significative.
Plus tard, après plusieurs années, la resténose reste possible par progression de la maladie athéromateuse, donnant alors des images plus banales de plaques. Les altérations de la paroi au niveau d’une anastomose sont plus exceptionnelles, donnant naissance à une ectasie localisée ou à un faux-anévrisme.